Comment ça fonctionne ?
Le fonctionnement d'une voiture à dihydrogène est très simple. Dès lors que la voiture est allumée, le dihydrogène est envoyé dans la pile à combustible. Le dihydrogène sous pression est mis au contact du dioxygène de l'air. Les deux éléments se combinent pour se transformer en H20, l'eau, et produire de l'électricité. La vapeur d'eau est rejetée par le pot d'échappement tandis que l'électricité alimente le moteur.
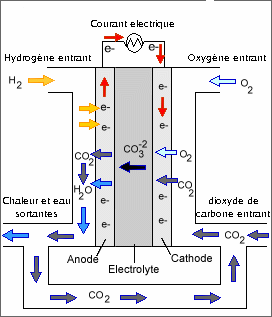
La pile à combustible fonctionne sur le principe de la synthèse de l'eau. Les molécules de dihydrogène se séparent (bleu), les électrons (rouge) partent par un circuit annexe et fabriquent l'électricité nécessaire grâce à du dioxygène (vert). Les protons qui traversent la membrane se recomposent avec les électrons qui reviennent et avec le dioxygène de l'air pour fabriquer de l'eau.
Explication : la pile à combustible
Les différentes piles à combustibles :
La pile à combustible dite PAC est un générateur d’électricité transformant l'énergie d'une réaction chimique. Elle est composée d’une anode, d'une cathode, de deux catalyseurs (backing sur le schéma), de deux plans d’écoulement ou plaques bipolaires et d’un électrolyte dit PEM.
Il existe cinq piles à combustibles différentes qui dépendent principalement du type d’électrolyte utilisé. Le type de pile employé dépend de l'utilisation de la machine :


La pile SOFC :
SOFC signifie Solid oxide fuel cells : pile à combustible à oxyde solide : Cette pile peut utiliser 2 types de comburants : le dihydrogène (H2) et le monoxyde de carbone (CO). Les SOFC utilisent comme électrolyte du Zirconium (Zr^2+) ainsi que de l’Ytterbium (Y^3+) permettant le passage des anions oxygène (O^2+) :
Réaction à l’anode :
2 H2 + 2 O2- → 2 H2O + 4 e- pour le dihydrogène ou
2 CO + 2 O2-→ 2 CO2 + 4 e- pour le monoxyde de carbone.
Réaction à la cathode : O2 + 4 e- → 2 O^2-
La température de fonctionnement est de l’ordre de 600 à 1000°C ce qui peut être un avantage dans un cas de cogénération avec l’électricité et la chaleur. De plus, cette pile a un rendement énergétique atteignant 80%. Cependant cette forte température prend du temps à se produire et ne peut être utilisée dans des cycles courts comme les transports.
La pile AFC :
AFC signifie alkaline fuel cell : pile à combustible alcaline utilisant l dihydrogène comme combustible et l’air comme oxydant. La température de fonctionnement est d’environ 120 à 150 °C. Elle utilise comme électrolyte de l'hydroxyde de potassium KOH, généralement en concentration de 30 à 40%. Le KOH est employé car il est conducteur des ions HO- (hydroxyde) créés par les réactions suivantes :
A l’anode: 2 H2+ 4 HO- → 4 H2O + 4 e-
A la cathode: O2 + 4 e- + 2 H2O→4 HO-
Elles ont un rendement énergétique d’environ 70 %. Cependant ces ions peuvent réagir dans l’électrolyte avec le dioxyde de carbone CO et former du carbonate ce qui baisse fortement son rendement en bouchant l’électrolyte car il se fixe à celui -ci.
CO2+ 2 OH-→ (CO3)^2–
C’est pourquoi ces piles sont principalement utilisées par la NASA dans l'espace compte tenu de l’absence de dioxyde de carbone.
La pile MCFC :
MCFC signifie Molten-carbonate fuel cell : pile à combustible à carbonate fondu. L’électrolyte de cette pile est formée à partir de métaux alcalins ainsi qu’une matrice céramique d’oxyde d’aluminium et de lithium. La température de fonctionnement atteint les 600°C et possède un rendement énergétique de 70% si cette chaleur est recyclée. Toutes sortes de comburants peuvent être utilisées directement dans la pile pour ainsi réduire les coûts de productions grâce au reformage interne. Elle possède les mêmes inconvénients que la SOFC compte tenu de sa chaleur. C’est pourquoi elle a aussi un usage stationnaire. Les réactions mises en jeu sont :
A l’anode :2 H2+2 CO3^2-→ 2H2O + 2 CO2 + 4 e-
A la cathode:O2+ 2 CO2 + 4 e- → 2 CO3^2-
La pile PAFC :
PAFC signifie phosphoric acid fuel cells : pile à combustible à acide phosphorique. Cette pile fonctionne de la même manière que la PEMFC présentée ci-dessous. Cependant, l’électrolyte est composé d’acide phosphorique liquide. Sa température de fonctionnement est de 150 à 200 °C. La température de fusion de l’acide phosphorique est de 40°C, c’est pourquoi la pile doit être utilisée en continu pour des actions industrielles de telle sorte qu’elle ne se solidifie pas.
La pile PEMFC :
PEMFC signifie proton exchange membrane fuel cells : pile à combustible à membrane d'échange de protons. Celles-ci utilisent aussi le dihydrogène comme combustilble ainsi que l'air comme oxydant. Cependant la compostition de l'électrolyte n'est pas la même. En effet, il est constitué de Nafion, un matériau laissant passer seulement les ions hydrogène, la température avoisine les 80°C de telle manière qu'elle garde la membrane humide.
Réaction sur l'anode : H2 → 2H+ +2e
Réaction sur la cathode : O2 + 4H+ + 4e- → 2H2O
Il existe aussi une variante à la pile PEMFC, où le combustible est le méthanol d'où son nom DMFC : pile à combustible méthanol-direct elle possède la même composition et la température ne dépasse pas les 80°.Etant donné la faible température de fonctionnement de la PEMFC, elle peut être utilisée pour des cycles cours comme les transports, cette pile est par conséquent utilisée dans les voitures à hydrogène et peut être aussi employée pour les utilisations stationnaires et portables.

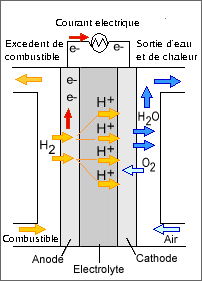
Particularité de la pile PEMFC :
Comme nous l'avons vu précédement, la pile PEMFC est la pile la plus convenable pour des utilisations en cycle court et elle est par conséquent la pile la plus utilisée dans la fabrication de voitures à hydrogène. Cette pile a aussi la particularité de ne rejeter que de l'eau alors que d'autres piles peuvent rejeter du dioxyde de carbone. Elle est composée d'une membrane en Nafion servant d'élelectrolyte. Comme c'est une membrane, elle est organique. Ce matériau a de nombreuses contraintes qu'il faut prendre en compte pour des questions de sécurité et de rendement :
-
Conduction protonique élevée pour assurer le transfert des protons de l’anode à la cathode
-
Isolant électrique pour éviter le court-circuit
-
Faible perméabilité gazeuse afin d’éviter la rencontre directe de H2/O2, dont la réaction est explosive
-
Bonne stabilité mécanique pour éviter une différence de pression éventuelle entre anode et cathode
-
Bonne stabilité chimique pour résister à la dégradation
C'est pourquoi le Nafion a une structure complexe constituée principalement d'un polymère carboné perfluoré, ( en effet, tous les atomes d'hydrogène sont remplacés par des atomes de fluor ), avec des groupements sulfonés, ce qui rend le Nafion acide.

Groupement sulfoné
Formule développée du Nafion
Pour le groupement sulfoné, on peut voir sur la formule du Nafion que R=OH et R' représente le reste de la formule. Aussi, pour que la réaction d'oxydoréduction (réaction chimique au cours de laquelle se produit un échange d'électrons) aille plus vite, deux catalyseurs en platine sont utilisés de part et d'autres de l'électrolyte. En effet, le platine est à ce jour le seul catalyseur capable de se situer dans un milieu acide sans se corroder et jouer son rôle d'accélérateur.
Aussi pour que le rendement énergétique soit maximal, les matériaux utilisés pour les plaques bipolaires sont aussi importants. Pour ce qui est de la PEMFC, elle utilise des métaux et des alliages, et particulièrement des aciers inoxydables car ceux-ci présentent un ensemble de propriétés (tenue mécanique, étanchéité, conductivité électrique, aptitude à la mise en forme par des procédés de production de masse) qui en font des candidats de choix pour la conception et la réalisation de ces plaques bipolaires compactes. Ainsi, ces plaques ont une durée de vie de 3000 à 5000 heures pour une application automobile.
Il ne faut pas non plus oublier la structure de la plaque bipolaire. Il en existe de différentes
formes mais pour avoir le meilleur rendement énergétique possible, la structure en serpentins
est la plus utilisée car aucun canal n’est fermé ce qui rend plus difficile la formation d’un
bouchon dans l'écoulement du dihydrogène.

Structure en serpentins d'un plan d'écoulement

Pour qu'une pile PEMFC produise suffisament d'énergie ( environ 75 kW pour une voiture à hydrogène), il est nécessaire de superposer les piles comme le montre la photo ci-contre pour ainsi accumuler l'énergie nécessaire à l'alimentation du moteur électrique. En effet, chaque piles délivrent une puissance de 2 W/cm² environ.
